Новое руководство Европейского агентства по лекарственным средствам по медицинским устройствам направлено на оптимизацию процедур, но интеграция технологий в системы здравоохранения остается сложной задачей, предупреждают представители польской промышленности.
Европейское агентство по лекарственным средствам (EMA) опубликовало новую версию рекомендаций по медицинским изделиям и диагностике in vitro. Теперь он доступен заявителям, держателям регистрационных удостоверений и нотифицированным органам в области медицинских изделий.
Польская торговая палата медицинского оборудования POLMED заявила: «Новые рекомендации улучшат понимание и реализацию относительно новых правил в отношении медицинских устройств и медицинских устройств для диагностики in vitro».
«Как рекомендации EMA, так и ранее выпущенные рекомендации Координационной группы по медицинскому оборудованию (MDCG) способствуют большей гармонизации правил во всех государствах-членах ЕС», — сообщили в POLMED Euractiv.
Медицинское оборудование
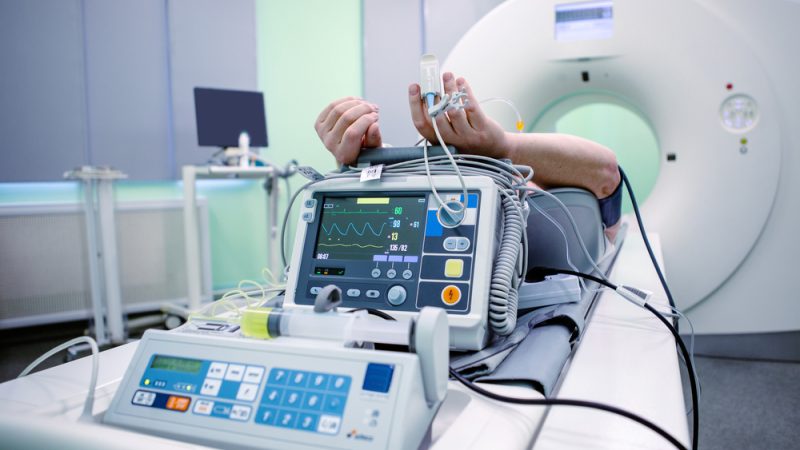
Категория медицинских устройств включает инструменты, инструменты, машины или имплантаты, используемые в здравоохранении для диагностики, предотвращения, мониторинга или лечения заболеваний и заболеваний. Они варьируются от простых предметов, таких как бинты и термометры, до сложных технологий, таких как кардиостимуляторы, аппараты МРТ и даже роботы, выполняющие сложные хирургические операции.
«Эти медицинские устройства способствуют выздоровлению пациентов, предотвращают социальную изоляцию и помогают преодолеть барьеры повседневной жизни», — сказал Euractiv Аркадиуш Грондковский, президент Палаты POLMED и член правления MedTech Europe.
«Короче говоря, они обеспечивают максимально возможную функциональность и качество жизни, защищают конфиденциальность и гарантируют достоинство», — добавил он.
Сектор медицинского оборудования также является второй наиболее инновационной отраслью в Европе.
Принято считать, что в мире доступно более 2 миллионов различных типов медицинских устройств. Эти устройства разделены на более чем 22 000 общих групп, что отражает огромное разнообразие и специализацию медицинских технологий.
В Польше доступно около 300 000 медицинских изделий. Многие из них играют решающую роль в ускорении процесса выздоровления и повышении качества жизни пожилых людей, многие из которых страдают от множества заболеваний.
Ожидается, что по мере старения населения спрос в этой области значительно вырастет, что сделает доступ к этим устройствам еще более важным.
Проблемы реализации в Польше
Хотя медицинские устройства имеют широкий спектр применения, узким местом в их использовании является внедрение в системы здравоохранения.
Основной проблемой является отсутствие четко определенных путей интеграции медицинских изделий в систему общественного здравоохранения.
Этот процесс еще больше усложняется разнообразием медицинских устройств, которые сильно различаются даже в пределах одной и той же группы продуктов и постоянно развиваются и совершенствуются.
Грондковский считает, что для того, чтобы пациенты имели хороший доступ к широкому спектру новейших медицинских технологий, «нам нужно четкое, прозрачное и предсказуемое законодательство». Он указывает на две ключевые проблемы, которые необходимо решить.
Во-первых, в настоящее время подать заявку может только национальный консультант или государственная администрация. Решением могло бы стать разрешение производителям медицинского оборудования также подавать заявки.
Эти производители владеют важной информацией о своей продукции, включая результаты исследований и исследований. По мнению Грондковского, это изменение значительно сократит весь процесс.
Во-вторых, отсутствие четко определенных временных рамок для каждого этапа процесса подачи заявки означает, что процедуры часто ждут годы, прежде чем они будут внедрены в общее пользование.
«Учитывая, как быстро развивается отрасль, справедливо сказать, что польские пациенты получают эти технологии, когда они уже не являются инновационными», — сказал Грондковский. Установление конкретных сроков для каждого этапа процесса рассмотрения заявок обеспечит, чтобы вся процедура занимала не более трех месяцев.
Межминистерская тема
Кроме того, необходимо регулярно обновлять список медицинских изделий, отпускаемых по рецепту, как с точки зрения входящих в них препаратов, так и с точки зрения расширения лимитов финансирования. В этом процессе должны участвовать организации, представляющие пациентов, национальных консультантов, научные общества и промышленность.
«В настоящее время не существует законодательной процедуры, обеспечивающей регулярное информирование лиц, принимающих решения», — сказал Грондковский.
В Польше также нет специального отдела в Министерстве здравоохранения, который занимался бы медицинскими устройствами. Поэтому «внедрение медицинских изделий в систему здравоохранения должно стать темой межминистерских дискуссий», — заявила на конференции 10 июня профессор Агнешка Нойманн-Подчаска, директор Национального института гериатрии, ревматологии и реабилитации. 2024.
[By Paulina Mozolewska, Edited by Vasiliki Angouridi, Brian Maguire | Euractiv’s Advocacy Lab]
Узнайте больше с Euractiv

 EUROPEAN UNION
EUROPEAN UNION 