Система для введения белка непосредственно в мозг. Фото Physorg
Многие знают о таком нейродегенеративном заболевании, как рассеянный склероз. Оно вызывается атакой собственных Т-лимфоцитов на миелиновые оболочки нервных отростков. Лечат его диметил-фумаратом, представляющим собой эфир фумаровой кислоты, участвующей в клеточном энергообмене.
Как сообщает журнал Nature Materials, для более безопасного лечения мозговых заболеваний в Гарварде предложили импланты, ведущие себя подобно нейронам. Электроника, имитирующая нервные клетки, представляет собой симбиоз с мозговой тканью. Это позволяет осуществлять 3D-картирование нейронов и клеток белого вещества – глии («клея»). Они взаимодействуют с имплантом в формирующемся интерфейсе. Имплант с металлическим электродом, записывающим нервную активность, имитирует форму нервной клетки, а его полимерный «хвост» дополняет сходство. Статья гарвардцев называется «Биовдохновленная (bioinspired) нейроноподобная электроника». В ней также говорится, что электронные «нейроны» стимулируют миграцию нервных стволовых клеток (НСК).
Кстати о НСК, предшественники которых сидят в… костном мозге. В медцентре Сидар-Синай, что в Западном Голливуде, с целью омоложения предприняли пересадку костного мозга, благодаря чему у мышей-реципиентов «оживилось» их собственное кроветворение. Затем последовало укрепление синапсов на фоне снижения активности клеток микроглии, выполняющей в мозге роль иммунных лимфоцитов. В 2018 году журнал New Scientist уже сообщал о лечении 90 паркинсоников в возрасте 70–80 лет и людей с болезнью Альцгеймера переливанием им крови молодых людей.
Нейровоспаление опасно для клеток сетчатки глаза, поэтому понятен интерес специалистов к методам избавления от слепоты. Сотрудники Массачусетского технологического института сообщали в конце 2015 года, что им удалось создать квантовые точки, преобразующие инфракрасный свет в видимый. Но тогда идея не получила развития. На этом фоне иной эффект имело сообщение о получении наночастиц, которые связываются с фоторецепторами сетчатки – палочками и колбочками, – преобразуя видимый свет в инфракрасный. Это позволило подопытным мышам различать круги и треугольники. Работа осуществлена специалистами Университета науки и технологии в г. Хефей китайской провинции Анхой.
Наночастицы поглощали инфракрасный свет с длиной волны 980 нанометров (нм) и преобразовывали его в зеленый (535 нм). Подобная конверсия расширила диапазон видимости для мышей, которые, как и человек, инфракрасную часть спектра не способны воспринимать непосредственно. Думается, что слепые люди не откажутся от возможности видеть, используя принцип работы приборов ночного видения, реагирующих на что-то теплое.
 |
|
Чип с двумя антителами (голубым и розовым в левом верхнем квадрате). Фото Physorg |
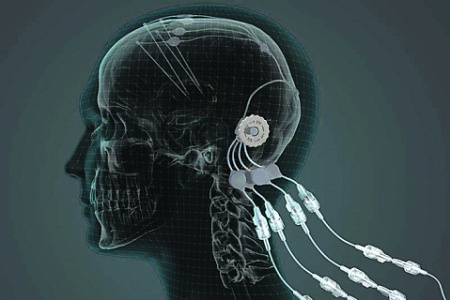
Еще с большим интересом воспринимается информация о прямом введении в мозг нейро-трофического фактора, который поддерживает жизнеспособность дофаминовых нейронов. Речь идет о GDNF, или Glial-Derived Neurotrophic Factor (протеиновый фактор, вырабатываемый в мозге его глиальными кулетками), и нейронах, синтезирующих из аминокислоты тирозина дофамин, нехватка которого приводит к паркинсонизму. Дофамин необходим для поддержания жизнеспособности клеток подкорковых ядер мозга, контролирующих сокращение мышц и движения головы и конечностей. Сама система, опробованная на 41 пациенте, была создана специалистами Бристольского университета.
GDNF вводили в мозг 41 паркинсоника в возрасте 35–75 лет через укрепленный за ухом «порт», снабженный противомикробным фильтром. Сканирование мозга показало большую активность нервных клеток после введения GDNF. Лечение, которое было малоэффективным после 40 недель, продолжалось в течение девяти месяцев, и врачи отметили уменьшение тремора, а также то, что люди начали ходить самостоятельно. Английские ученые надеются, что дальнейшее улучшение введения других нейротрофических факторов, а возможно и самого дофамина обеспечит их устройству клиническую жизнь.

